Unter den Grundgesetzen der Thermodynamik nimmt das nullte Gesetz eine entscheidende Stellung ein, da es die grundlegenden Konzepte der Temperatur und des thermischen Gleichgewichts festlegt.
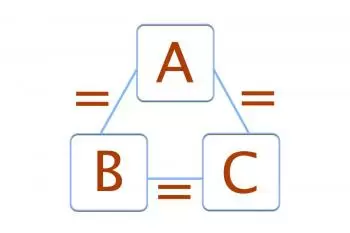
Der nullte Hauptsatz der Thermodynamik besagt: „Wenn zwei Systeme mit einem dritten System im thermischen Gleichgewicht stehen, stehen sie auch untereinander im Gleichgewicht.“ Es ist auch als Nullprinzip der Thermodynamik bekannt.
Wenn A mit B im Gleichgewicht steht und A auch mit einem dritten Körper C im thermischen Gleichgewicht steht, können wir daraus schließen, dass B mit C im thermischen Gleichgewicht steht.
Zwei Körper befinden sich im thermischen Gleichgewicht, wenn sich ihre Zustandsgrößen bei Kontakt nicht ändern. Befinden sie sich nicht im thermischen Gleichgewicht, unterliegen sie einem Wärme- oder Energieaustausch und erreichen das thermische Gleichgewicht.
Der nullte Hauptsatz war der letzte Hauptsatz der Thermodynamik, der eingeführt wurde. Um eine logische Struktur zu erhalten, war es notwendig, es vor die anderen Gesetze zu stellen.
Formel des 0. Hauptsatzes der Thermodynamik
Prinzip 0 der Thermodynamik: Wenn sich die drei Systeme im thermischen Gleichgewicht befinden, muss die folgende Formel vervollständigt werden:
TA = TB = TC
Dabei sind TA , TB und TC die Temperaturen der drei Systeme.
Ursprung und Geschichte des Nullgesetzes
Der nullte Hauptsatz der Thermodynamik wurde als Antwort auf Fragen zum Messen und Vergleichen von Temperaturen formuliert. Vor ihrer Einführung waren Temperaturskalen willkürlich und von bestimmten Messmethoden abhängig. Der Bedarf an einer solideren Grundlage für den Temperaturvergleich war ein heißes Thema in der wissenschaftlichen Gemeinschaft des 19. Jahrhunderts.
Es war der deutsche Physiker Gustav H. Johannsen, der in den 1860er Jahren erstmals die zentrale Idee des Nullten Gesetzes formulierte, doch erst in den 1930er Jahren wurde sie gefestigt und als Grundgesetz der Thermodynamik aufgenommen.
Das nullte Gesetz wird so genannt, weil es die Grundlage für die Konstruktion von Temperaturskalen bildet und ein Grundprinzip für die Temperaturmessung festlegt.
Beispiele für das nullte Gesetz
Um zu verstehen, wie der nullte Hauptsatz der Thermodynamik funktioniert, schlagen wir drei Beispiele vor:
Eis und Wasser
Wir stellen ein Stück Eis und ein Glas Wasser auf Zimmertemperatur. In diesem Experiment erscheinen drei Elemente: Eis, Wasser und das Glas.
Zunächst tauschen die drei Wärme und Energie aus, bis ein thermisches Gleichgewicht erreicht ist. Nach einiger Zeit erreichen die drei Elemente die gleiche Temperatur
Tassen Kaffee
Stellen wir uns zwei Tassen Kaffee vor, eine heiße und eine kalte. Wenn sie in Kontakt kommen, fließt Wärme von der heißen Tasse zur kalten Tasse, bis beide die gleiche Temperatur erreichen und sich im thermischen Gleichgewicht befinden.
Dies ist ein praktisches Beispiel für die Wirkung des Nullprinzips: Die beiden Systeme befinden sich im thermischen Gleichgewicht, wenn zwischen ihnen keine Nettowärmeübertragung mehr stattfindet.
Beispiel für ein Thermometer
Ein weiteres Beispiel, das zum besseren Verständnis des Konzepts des thermischen Gleichgewichts beiträgt, ist das eines Thermometers.
Stellen Sie sich einen Körper B vor, der aus einem Rohr mit einer Kapillare besteht, die Quecksilber enthält. Ihre Höhenniveaus über der Kapillare repräsentieren unterschiedliche Temperaturen.
Betrachten Sie nun einen Körper A, zum Beispiel den menschlichen Körper. Wenn Sie das Thermometer nahe an Ihren Körper bringen und lange genug dort belassen, erreicht das Thermometer den Wert, der Ihrer Körpertemperatur entspricht.
Das Thermometer und der menschliche Körper stehen miteinander im thermischen Gleichgewicht. Daher erreichen beide Elemente die gleiche Temperatur.